京都大学5月28日宣布,钙反应诱发癌细胞释放PGE2,而这种钙反应是血管内皮细胞响应血管内皮生长因子刺激而分泌的A2 (TXA2) 作用于肿瘤细胞。这项研究是由同大大学院生命科学研究科松田道行教授、同大医学研究科寺井健太准教授、小西義延同研究員组成的研究小组进行的。研究结果发表在线上版的“癌症研究”上。
癌细胞通过改变周围的肿瘤微环境并通过释放抑制免疫系统的物质和吸引抑制免疫系统的细胞来抑制免疫系统而存活下来。这种免疫逃脱已成为癌症治疗中的一个重要问题。
PGE2是癌细胞释放的典型物质,具有抑制免疫力的作用,一段时间以来一直备受关注。然而,调节癌细胞释放PGE2的机制尚未完全阐明。因此,研究小组进行了研究,旨在阐明控制癌细胞释放 PGE2 的细胞之间的相互作用。
细胞内 PGE2 的产生是由钙反应触发的。因此,我们观察了活体小鼠癌细胞的钙反应,并试图通过给药和基因修饰技术阐明 PGE2 释放的控制机制。
由于活体组织不容易让光线通过,因此使用具有良好组织渗透性的双光子显微镜观察移植到小鼠皮下的癌细胞。结果,在肿瘤微环境中(体内)的一些癌细胞中观察到了活跃的钙反应。在癌细胞单一培养物(体外)中未观察到钙反应,表明钙反应是由癌细胞与其他细胞之间的细胞间相互作用引起的。
接下来,我们在癌细胞上寻找在癌细胞中引发钙反应的受体。结果阐明,缺乏TXA2受体的癌细胞的钙反应受到抑制,肿瘤微环境中PGE2的浓度降低,达到了免疫清除癌细胞的目的。
此外,发现通过施用血管内皮生长因子的特异性抑制剂降低了肿瘤微环境中的TXA2浓度和PGE2浓度。
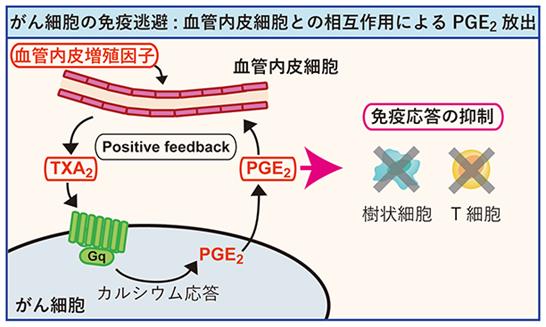
由这些结果可知,血管内皮细胞因血管内皮生长因子的刺激而释放的TXA2诱导癌细胞的钙反应,促进PGE2的释放,抑制免疫。
对新的癌症免疫疗法发展的期望
少数临床试验报道了抑制血管内皮生长因子以增强对癌症的免疫反应。本研究的结果阐明了这种临床效应的部分分子机制。
该研究小组表示,预计这项研究的结果将导致新的癌症免疫疗法的开发,包括与其他免疫疗法(如免疫检查点抑制剂)的组合。






请您简单描述您正面临的问题和您的需求,并留下您的联系方式;
我们会为您匹配专门的医学顾问与您联系,帮你制定合适的方案。
在您提交相关的信息后,我们将会由专业的医学团队帮您规划合适的出国看病方案并进行费用预估。